진흥원, 블록버스터 의약품 특허 만료‧장려 정책 등 바이오시밀러 성장 요인
글로벌 비만치료제 시장 2023년 1000억 달러 예상…디지털헬스 기업 가세
[의학신문·일간보사=정광성 기자] 글로벌 제약바이오 시장에서 바이오시밀러‧비만치료제 시장이 빠른 속도로 성장하며 차세대 먹거리로서 주목받고 있는 것으로 나타났다.
보건산업진흥원은 최근 ‘글로벌 제약바이오산업 동향 Vol.1’ 창간 보고서를 통해 글로벌 제약바이오 산업의 최신동향을 공유했다.
Recearch and Marketsd의 올해 초 연구에 따르면 글로벌 바이오시밀러 시장은 지난 2021년 156억 7000만 달러에서 지난해 191억 달러 규모로 연평균 21.8% 성장했으며, 오는 2026년까지 연평균 22% 성장해 423억 달러에 달할 것으로 예상했다.
진흥원은 “이는 생물학적 약물에 대한 저비용 대안에 대한 수요 증가와 바이오시밀러에 대한 규제지원, 의료서비스 제공자와 환자의 바이오시밀러 수용도 증가에 의한 것”이라고 평가했다.
실제 2032년까지 존슨앤존슨, 다케다, 아스트라제네카, 로슈 등 연 매출 10억 달러가 넘는 55개의 블록버스터급 바이오 의약품의 특허가 만료될 예정이며, 해당 바이오시밀러의 최대 예상 매출은 2700억 달러에 달할 것으로 전문가들은 추청하고 있는 상황.
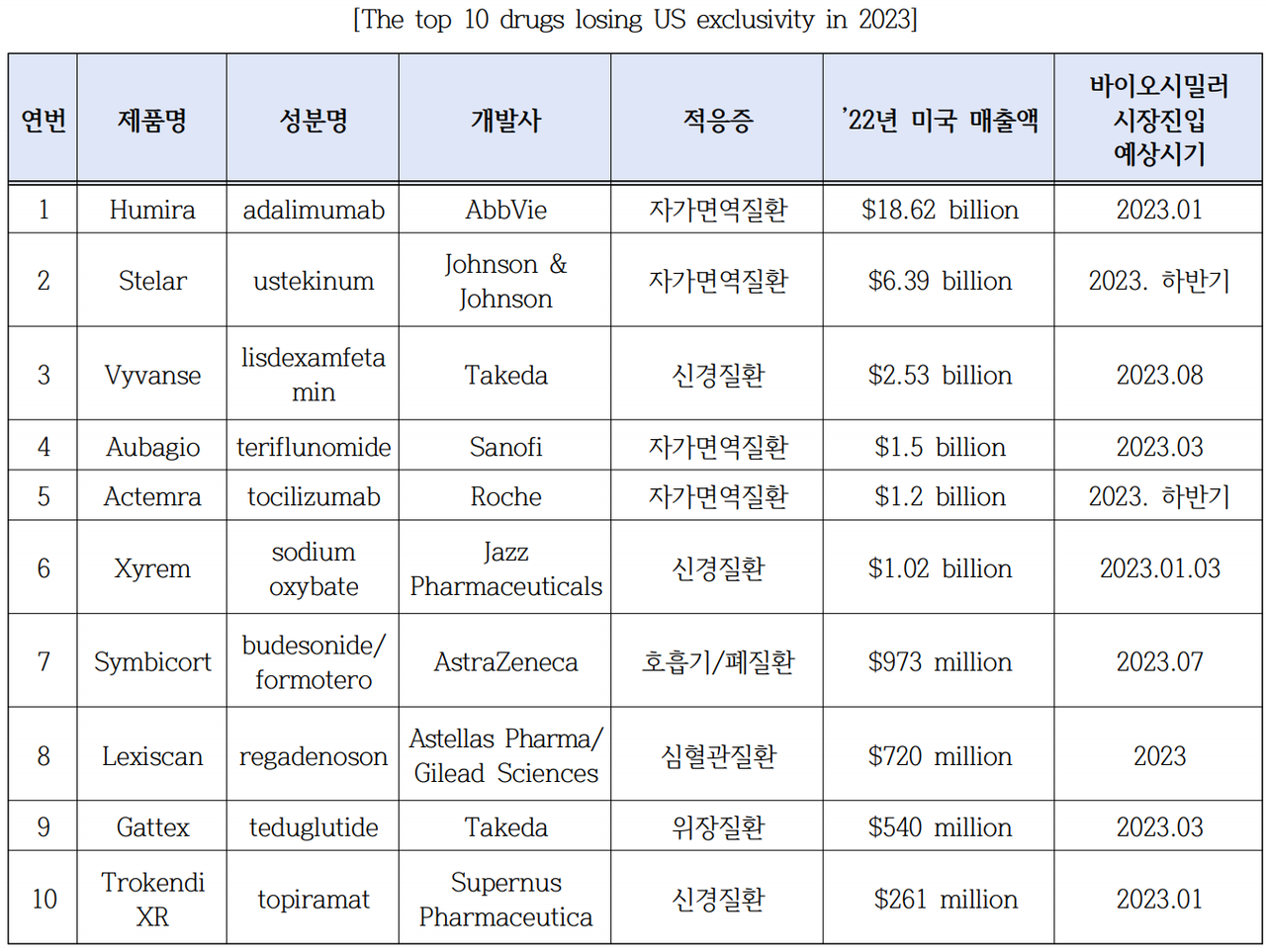
진흥원은 이와 더불어 미국‧유럽 등 보험재정 절감을 위한 바이오시밀러 처방 장려 추세에 따라 바이오시밀러 시장이 더욱 활성화될 것으로 내다봤다.
또한 지역별로는 유럽이 바이오시밀러 시장에서 가장 높은 점유율을 차지하고 있는 것으로 파악됐다.
유럽은 지난 2006년 최초의 바이오시밀러 승인을 시작으로 2021년까지 50% 이상의 시장 점유율을 차지하고 있으며, 규제 당국의 바이오시밀러 의약품 승인을 위한 적절한 제도 마련으로 도입이 증가해 시장 성장이 가속화되고 있다.
미국도 글로벌 제약사의 특허전략 등으로 성장이 더뎠으나 지난 2015년 암젠의 뉴포젠 바이오시밀러 산도스의 자시오 승인 이후 2021년까지 연평균 97%의 성장률을 보이며 빠르게 성장 중이다.
하지만 유럽은 EU에서 허가된 모든 ‘바이오시밀러-오리지널의약품’과 ‘바이오시밀러-바이오시밀러’ 상호 교체가 가능함을 명문화한 반면 미국은 바이오시밀러 제품이 상호 교환 가능상태를 충족하기 위해 FDA에 추가 데이터 제출이 필요한 상황이다.

올해 4월 기준 EMA는 19개 바이오의약품에 대한 75개 바이오시밀러를 승인했으나, FDA는 11개 바이오의약품에 대해 40개의 바이오시밀러를 승인하는 등 차이를 보였다.
이에 미 보건복지부는 하원에 메디케어 내에서 바이오시밀러 접근성을 개선할 시범 프로젝트를 수립하는 ‘바이오시밀러 접근성 향상법’을 제출했다.
진흥원은 “주요 블록버스터 약물들의 특허 만료 및 2023년 바이오시밀러 접근성 향상법 하원 제출 등의 이벤트로 미국 시장이 크게 성장할 것”이라고 예상했다.
글로벌 비만치료제 시장 2030년 1000억 달러 전망
한편 진흥원은 현대인의 생활 습관 변화‧새로운 치료법 등의 등장으로 향후 몇 년간 지속적 성장을 거듭해 글로벌 비만치료제 시장은 오는 2030년 1000억 달러에 이를 것으로 전망했다.
구체적으로 △비만 인구의 증가 △효율성‧지속성이 탁월한 치료법 증가 △경구용 글루카곤 출시 등 새로운 치료법의 대두를 주요 요인으로 지목했다.
실례로 중국 기관지인 인민일보에 따르면 ‘중국 거주자의 영양 및 만성 질환 상태 보고서’에서 성인의 50%가 비만이었으며, 2020년 기준 중국의 예상 비만 인구는 2억 2000만 명으로 2025년에는 중국 비만치료제 시장이 120억 위안을 초과할 것으로 분석했다.
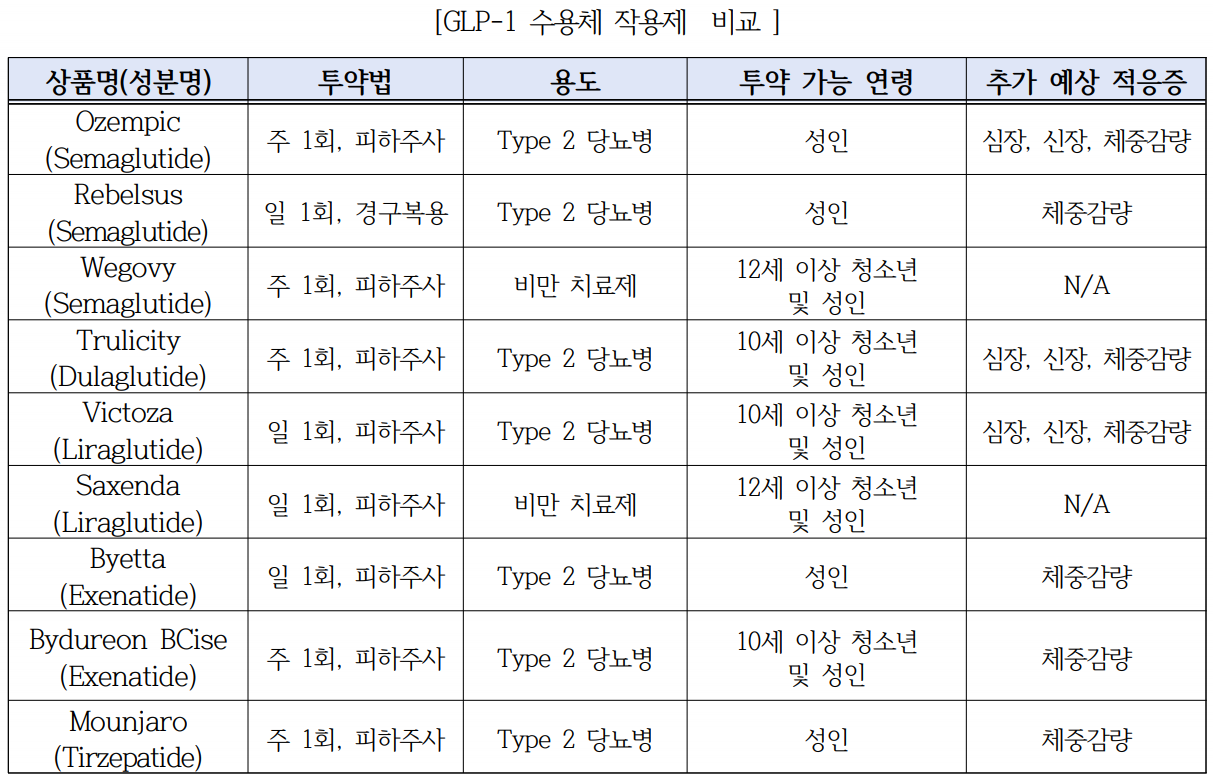
그동안 향정신성 약물이 주를 이루던 비만치료제 시장은 지난 2014년 노보 노디스크가 FDA로부터 ‘삭센다’를 비만 치료제로 승인받은 이후 전환점을 맞이해 2021년 ‘위고비’가 출시되는 등 GLP-1 기반 비만치료제가 각광받고 있다.
현재 노보 노디스크는 경구용 세마글루타이드 개발을 위한 임상 3상을 진행 중이며, 일라이 릴리는 지난해 당뇨병 치료제로 FDA 승인받은 GLP-1/GIP 이중 작용제 기반 비만치료제 ‘마운자로’의 임상을 진행 중이다.
국내에선 한미약품이 GLP-1 작용제 ‘에페글레나타이드’, 삼중작용제 ‘랩스 트리플 아고니스트’를 개발 중이다.
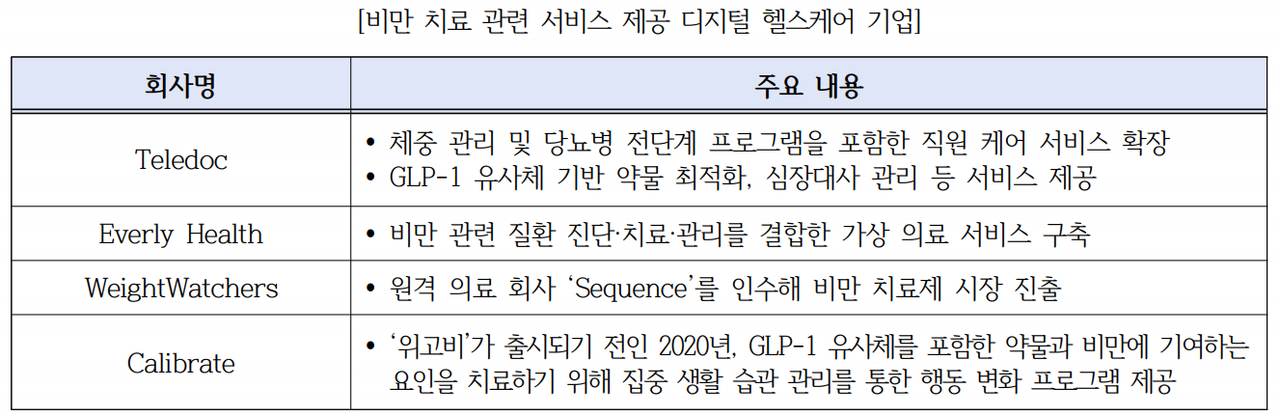
또한 시장 성장에 주목한 주요 디지털헬스 기업들도 비만 치료제 시장에 뛰어들고 있다. 대표적으로 텔레닥은 GLP-1 유사체 기반 약물 최적화‧심장대사 관리 등 서비스 제공에 나섰으며, 웨이트와처스는 원격의료회사 ‘시퀀스’를 인수해 비만 치료제 시장에 진출했다.
반면 美보험회사들의 비만치료제 수요가 증가와 복용기간‧부작용 등에 따른 보험적용기피 현상은 시장의 성장에 다소 걸림돌이 될 것으로 보인다.
진흥원은 “다수 디지털헬스케어 기업들이 비만치료제 시장에 진입하는 등 늘어나는 수요 증가에 대응하고 있으나 미국 주요 보험사들은 복용기간과 부작용 등을 이유로 보험적용을 거부하고 있다”고 설명했다.

